AVISO
ANSM - Actualizado el: 24/01/2024
Nombre del medicamento
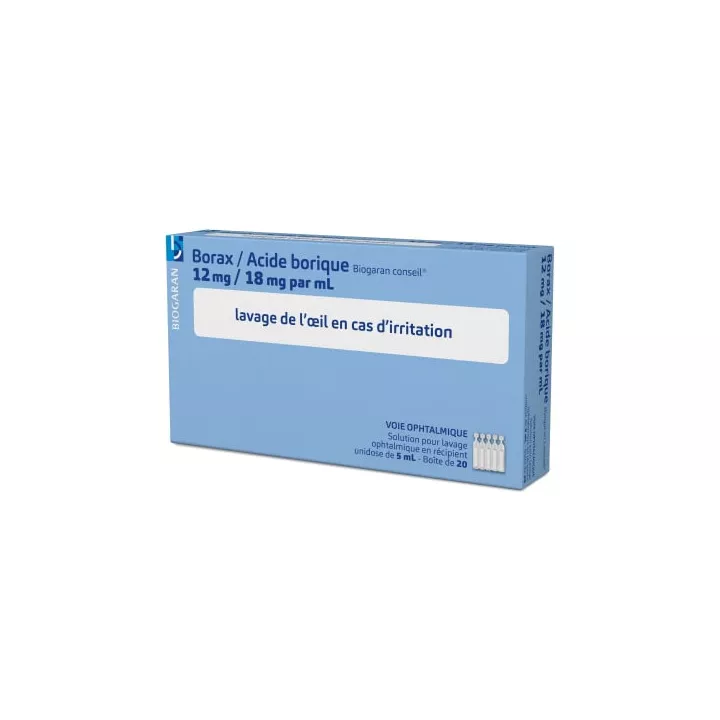
BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución para lavado oftálmico en envase monodosis
Bórax/Ácido bórico
Caja
- Lea este prospecto detenidamente antes de utilizar este medicamento, ya que contiene información importante para usted.
- Debe utilizar siempre este medicamento exactamente como se indica en este prospecto o como le haya indicado su médico o farmacéutico.
- Conserve este prospecto. Puede que necesite volver a leerlo.
- Pida consejo o información a su farmacéutico.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico. Esto también se aplica a cualquier efecto adverso no mencionado en este prospecto. Ver sección 4.
- Debe ponerse en contacto con su médico si no nota ninguna mejoría o si se siente peor.
- Mantenga este medicamento fuera del alcance de los niños.
¿Qué contiene este prospecto?
1. ¿Qué es BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis y para qué se utiliza?
2. ¿Qué debo saber antes de usar BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis?
3. ¿Cómo debo utilizar BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis?
4. ¿Cuáles son los posibles efectos secundarios?
5. ¿Cómo debo conservar BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis?
6. Contenido del envase y otra información.
1. ¿QUÉ ES BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis Y PARA QUÉ SE UTILIZA?
Clase farmacoterapéutica: ANTISEPTICO LOCAL / LIGHTASTRINGENTE DE USO OFTALMICO - Código ATC: S: órgano sensorial
Lavaojos en caso de irritación conjuntival.
2. ¿QUÉ NECESITA SABER ANTES DE UTILIZAR BORAX/VIATRIS ÁCIDO BÓRICO 12 mg/18 mg/mL, solución para lavado oftálmico en envase monodosis?
Nunca utilice BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución para lavado oftálmico en envase unidosis:
- Si es alérgico (hipersensible) al ácido bórico, al bórax o a cualquiera de los demás componentes de este medicamento, incluidos en la sección 6.
EN CASO DE DUDA, ES IMPRESCINDIBLE QUE CONSULTE A SU MÉDICO O FARMACÉUTICO.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envases unidosis.
No inyectar ni tragar.
Este producto puede utilizarse en pacientes que lleven lentes de contacto, pero es aconsejable quitárselas antes del lavado ocular.
Debido al riesgo de rápida contaminación bacteriana, un envase unidosis abierto no debe reutilizarse nunca para administraciones posteriores. Este producto no contiene conservantes.
Desechar el envase inmediatamente después de su uso.
En caso de problemas oculares, síntomas oculares inusuales, disminución de la agudeza visual o dolor ocular, debe solicitarse asistencia médica.
Si los síntomas persisten o empeoran, o si aparecen nuevos síntomas, interrumpa el tratamiento y consulte a un médico.
Niños y adolescentes
No aplicable.
Otros medicamentos y BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica para lavado en envase unidosis con alimentos, bebidas y alcohol
No aplicable.
Embarazo y lactancia
Este medicamento debe utilizarse con precaución durante el embarazo y la lactancia.
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de tomar este medicamento.
Deportistas
No aplicable.
Conducción de vehículos y uso de máquinas
Utilícelo con precaución cuando conduzca un vehículo o maneje maquinaria, ya que su visión puede ser borrosa inmediatamente después de su uso. En este caso, se aconseja no conducir ni utilizar maquinaria hasta que su visión vuelva a la normalidad.
BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envases unidosis contiene
No aplicable.
3. ¿CÓMO UTILIZAR BORAX/ÁCIDO BÓRBICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis?
Utilice siempre este medicamento exactamente como se lo haya recetado su médico o farmacéutico. Consulte a su médico o farmacéutico en caso de duda.
La dosis recomendada es de 1 a 3 lavados oculares al día.
El lavado se realiza directamente a chorro poniendo el envase unidosis boca abajo y presionando ligeramente sobre él, teniendo cuidado de que el envase unidosis no entre en contacto con la superficie del ojo y limpiando el exceso con una compresa o algodón.
Uso local.
COMO COLIRIO
Lavarse bien las manos.
Evitar tocar el ojo o los párpados con la punta del envase unidosis.
Puede utilizar el mismo envase para el tratamiento de ambos ojos.
Utilizar el envase inmediatamente después de abrirlo y desecharlo después de su uso.
No reutilice un envase abierto previamente.
Si está siendo tratado concomitantemente con colirios, espere 15 minutos antes de instilárselos.
Si ha utilizado más BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL de solución oftálmica en un envase unidosis del que debiera y observa cualquier efecto indeseable, aclare con solución salina estéril y consulte inmediatamente a su médico o farmacéutico. En caso de ingestión, acuda inmediatamente al médico o a un centro toxicológico.
Si olvidó usar BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis :
No aplicable.
Si deja de usar BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis :
No procede.
Si tiene cualquier otra duda sobre el uso de este medicamento, consulte a su médico o farmacéutico.
4. ¿CUÁLES SON LOS POSIBLES EFECTOS ADVERSOS?
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no siempre se dan en todas las personas.
Efectos adversos poco frecuentes (ocurren en 1 a 10 personas de cada 10.000):
- Irritación ocular
Notificación de efectos secundarios
Si experimenta algún efecto adverso, informe a su médico, farmacéutico o enfermero. Esto también se aplica a cualquier efecto adverso no mencionado en este prospecto. También puede notificar reacciones adversas directamente a través del sistema nacional de notificación: Agence Nationale de Sécurité du Médicament et des Produits de Santé (ANSM) y la red de Centros Regionales de Farmacovigilancia - Página web: https://signalement.social-sante.gouv.fr/
Al notificar reacciones adversas, está contribuyendo a proporcionar más información sobre la seguridad del medicamento.
5. CÓMO UTILIZAR BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envases unidosis
Mantenga este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad indicada en la caja o en el envase unidosis después de EXP. La fecha de caducidad se refiere al último día de ese mes.
Este medicamento no requiere precauciones especiales de conservación.
Después de su uso, el envase unidosis debe desecharse.
No reutilizar un envase unidosis abierto.
No tire ningún medicamento por el desagüe o con la basura doméstica. Pida a su farmacéutico que retire los medicamentos que ya no utilice. Estas medidas contribuirán a proteger el medio ambiente.
6. CONTENIDO DEL ENVASE Y OTRA INFORMACIÓN
Qué contiene BORAX/ÁCIDO BÓRICO VIATRIS 12 mg/18 mg/mL, solución oftálmica en envase unidosis
Los principios activos son :
Bórax.................................................................................................................................... 12 mg
Ácido bórico ....................................................................................................................... 18 mg
Por 1 mL de solución.
Los demás componentes son :
Cloruro de sodio, agua de rosas destilada, agua purificada.
Qué es BORAX/ÁCIDO BORIQUE VIATRIS 12 mg/18 mg/mL, solución para lavado oftálmico en envase unidosis y qué contiene
Este medicamento se presenta en forma de solución oftálmica.
Cajas de 10, 20 ó 30 envases monodosis de 5 mL.
No todas las presentaciones pueden comercializarse.
Titular de la autorización de comercialización
VIATRIS SANTE
1 RUE DE TURIN
69007 LYON
Titular de la autorización de comercialización
VIATRIS SANTE
1 RUE DE TURIN
69007 LYON
Fabricante
LABORATORIO UNITHER
151 RUE ANDRE DUROUCHEZ
ESPACE INDUSTRIEL NORD CS 28028
80084 AMIENS CEDEX 2
Nombre del medicamento en los estados miembros del Espacio Económico Europeo
No aplicable.
La última fecha de revisión de este prospecto fue el :
[a completar posteriormente por el titular].
Otros
La información detallada sobre este medicamento está disponible en la página web de la ANSM (Francia).