AVISO
ANSM - Actualizado el: 27/05/2025
Nombre del medicamento
MYCOSTER 1%, solución para aplicación cutánea
Ciclopirox olamina
Caja
Lea atentamente este prospecto antes de utilizar este medicamento, ya que contiene información importante para usted.
Debe utilizar siempre este medicamento exactamente como se indica en este prospecto o como le haya indicado su médico o farmacéutico.
- Conserve este prospecto. Puede que necesite volver a leerlo.
- Pida consejo o información a su farmacéutico.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico. Esto también se aplica a cualquier efecto adverso no mencionado en este prospecto. Ver sección 4.
- Debe ponerse en contacto con su médico si no nota ninguna mejoría o si se siente peor.
¿Qué contiene este prospecto?
1. ¿Qué es MYCOSTER 1%, solución para aplicación cutánea y para qué se utiliza?
2. ¿Qué debo saber antes de utilizar MYCOSTER 1%, solución para aplicación cutánea?
3. ¿Cómo debo utilizar MYCOSTER 1%, solución para aplicación cutánea?
4. 4. ¿Cuáles son los posibles efectos secundarios?
5. ¿Cómo debo conservar MYCOSTER 1%, solución para aplicación cutánea?
6. Contenido del envase y otra información.
1. ¿QUÉ ES MYCOSTER 1%, solución para aplicación cutánea Y PARA QUÉ SE UTILIZA?
Clase farmacoterapéutica: Antimicótico de uso tópico - Código ATC: D01AE14.
Este medicamento contiene el principio activo ciclopirox olamina que es un antifúngico cutáneo.
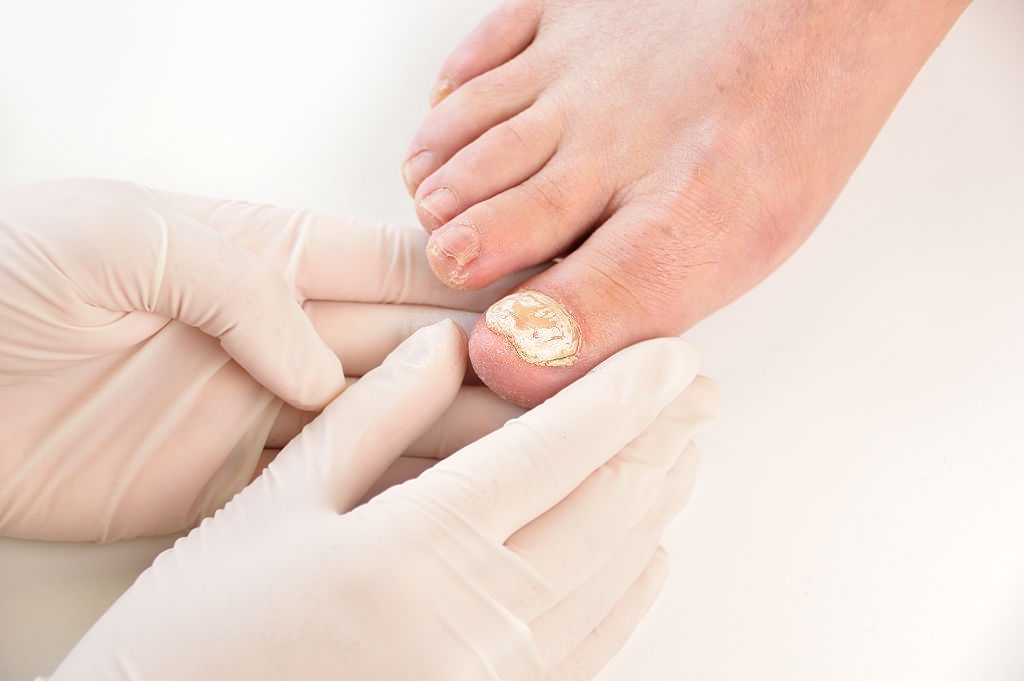
Este medicamento está indicado para el tratamiento de infecciones fúngicas (micosis) de la piel (dermatosis con o sin sobreinfección bacteriana) o de las uñas (onicomicosis).
2. ¿QUÉ DEBO SABER ANTES DE USAR MYCOSTER 1%, solución para aplicación cutánea?
No utilice nunca MYCOSTER 1%, solución para aplicación cutánea:
- si es alérgico a ciclopirox olamina o a cualquiera de los demás componentes de este medicamento mencionados en la sección 6.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar MYCOSTER.
- No tragar.
- Evitar el contacto con los ojos.
- Candidiasis (infección por hongos): no es aconsejable utilizar jabón con pH ácido, ya que favorece la multiplicación de la cándida (hongo).
- En caso de reacción alérgica, interrumpa inmediatamente el tratamiento, quítese cuidadosamente MYCOSTER y póngase en contacto con un médico.
Niños
No aplicable.
Otros medicamentos y MYCOSTER 1%, solución para aplicación cutánea
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
MYCOSTER 1%, solución para aplicación cutánea con alimentos y bebidas
No aplicable.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o está planeando quedarse embarazada, consulte a su médico o farmacéutico antes de tomar este medicamento.
Embarazo
No existen datos suficientes sobre el uso de ciclopirox olamina en mujeres embarazadas.
Como medida de precaución, es preferible evitar el uso de MYCOSTER durante el embarazo.
Lactancia
No existen datos suficientes sobre la excreción de ciclopirox olamina en la leche materna.
Como medida de precaución, es preferible evitar el uso de MYCOSTER durante la lactancia.
Conducción de vehículos y uso de máquinas
MYCOSTER no afecta a la capacidad para conducir y utilizar máquinas.
MYCOSTER 1%, solución para aplicación cutánea contiene
No aplicable.
3. ¿CÓMO UTILIZAR MYCOSTER 1%, solución para aplicación cutánea?
Utilice siempre este medicamento exactamente como se indica en este prospecto o como le haya indicado su médico o farmacéutico. Consulte a su médico o farmacéutico en caso de duda.
Posología
Micosis cutáneas: 2 aplicaciones diarias durante 21 días aproximadamente.
Micosis de las uñas: aplicar la solución sola o en combinación con otro tratamiento durante varios meses.
Método y vía de administración
Para uso cutáneo.
Sólo para uso externo.
Limpiar y secar las zonas a tratar.
Lávese bien las manos antes y después de cada aplicación.
Aplicar MYCOSTER en las zonas de la piel a tratar y masajear suavemente.
Si ha utilizado más MYCOSTER 1%, solución para aplicación cutánea del que debiera
No es aplicable.
Si olvida utilizar MYCOSTER 1%, solución para aplicación cutánea
No utilice una dosis doble para compensar la dosis que olvidó aplicar.
Si deja de usar MYCOSTER 1%, solución para aplicación cutánea
No es aplicable.
Si tiene cualquier otra duda sobre el uso de este medicamento, pida más información a su médico o farmacéutico.
4. ¿CUÁLES SON LOS POSIBLES EFECTOS ADVERSOS?
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no se dan sistemáticamente en todas las personas.
Efectos adversos frecuentes (pueden afectar hasta una de cada 10 personas)
- Empeoramiento temporal (durante un tiempo limitado) de ciertas reacciones adversas locales en el lugar de aplicación como enrojecimiento (eritema), picor (prurito) que generalmente es temporal y no requiere la interrupción del tratamiento.
- Sensación de quemazón.
Estos efectos indeseables pueden aparecer después de las primeras aplicaciones. Si estos síntomas persisten, consulte a un médico.
Reacciones adversas poco frecuentes (pueden afectar hasta 1 de cada 100 personas)
- Reacciones locales en forma de ampollas.
- Reacciones alérgicas generalizadas (hipersensibilidad) que pueden ser graves, durante las cuales puede experimentar hinchazón (edema), picor (prurito), una erupción en la piel que puede o no producir picor (urticaria) y dificultad para respirar (disnea). Si se producen estos efectos, debe dejar de tomar este medicamento inmediatamente y ponerse en contacto con un médico lo antes posible.
Frecuencia indeterminada (no puede estimarse a partir de los datos disponibles)
- Dermatitis de contacto (erupción parecida a un eczema).
Si aplica MYCOSTER durante un largo periodo de tiempo en una zona extensa, en piel dañada, en membranas mucosas o bajo un vendaje oclusivo (de cobertura), deben tenerse en cuenta los efectos del paso del medicamento al torrente sanguíneo: acuda al médico.
Notificación de efectos secundarios
Si experimenta efectos adversos, informe a su médico o farmacéutico. Esto también se aplica a cualquier efecto adverso no mencionado en este prospecto. También puede notificar reacciones adversas directamente a través del sistema nacional de notificación: Agence nationale de sécurité du médicament et des produits de santé (ANSM) y la red de Centros Regionales de Farmacovigilancia - Página web: https://signalement.social-sante.gouv.fr/.
Al notificar reacciones adversas, está contribuyendo a proporcionar más información sobre la seguridad de los medicamentos.
5. ¿CÓMO CONSERVAR MYCOSTER 1%, solución para aplicación cutánea?
Mantenga este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad indicada en el envase después de CAD. La fecha de caducidad se refiere al último día de ese mes.
Frasco de polietileno : No utilizar este medicamento una vez transcurrido 1 mes desde su primera apertura.
No tire ningún medicamento por el desagüe o con la basura doméstica. Pida a su farmacéutico que identifique los medicamentos que ya no utiliza. Estas medidas contribuirán a proteger el medio ambiente.
6. CONTENIDO DEL ENVASE Y OTRA INFORMACIÓN
Qué contiene MYCOSTER 1%, solución para aplicación cutánea
- El principio activo es :
Ciclopirox olamina............................................................................................................1,000 g
Por 100 ml de solución
- Los demás componentes son :
Macrogol 400, isopropanol, agua purificada.
Qué es MYCOSTER 1%, solución para aplicación cutánea y qué contiene
Este medicamento se presenta en forma de solución incolora o ligeramente amarilla para aplicación cutánea.
Frasco de vidrio o polietileno de 30 ml o 45 ml con tapón.
Titular de la autorización de comercialización
PIERRE FABRE MEDICAMENTO
LES CAUQUILLOUS
81500 LAVAUR
Titular de la autorización de comercialización
PIERRE FABRE MEDICAMENT
PARC INDUSTRIEL DE LA CHARTREUSE
81100 CASTRES
Fabricante
PIERRE FABRE PRODUCCIÓN DE MEDICAMENTOS
SITE PROGIPHARM
RUE DU LYCEE
45500 GIEN
Nombre del medicamento en los Estados miembros del Espacio Económico Europeo
No aplicable.
La última fecha de revisión de este prospecto fue el :
[a completar posteriormente por el titular].
Otros
La información detallada sobre este medicamento está disponible en la página web de la ANSM (Francia).